İzotop nedir? İzotop atom özellikleri ve atomların elektron sayısı nedir? İzotop atomların doğada bulunma yüzdeleri kaçtır? İşte izotop hakkında bilmeniz gereken bilgiler…
İzotop nedir?
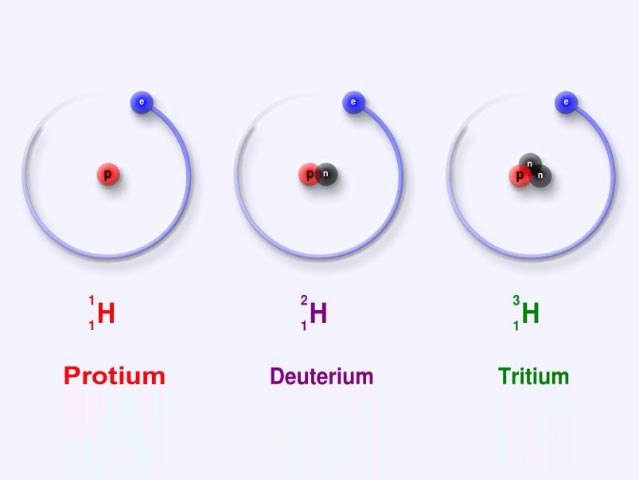
İzotop atom numarası aynı fakat kütle numarası farklı olan atomlara verilen isimdir. Bir maddenin tüm izotop sayısı her bir atomdaki proton sayısı ile eşittir. İzotop erimi Yunanca’da eşit anlamına gelen isos ve yer anlamına gelen topos kelimelerinin birleşiminden ortaya çıkmıştır. Bu da, tek bir maddenin farklı izotoplarının, periyodik tabloda aynı konumda yer almaları anlamını taşır.
İzotop atom özellikleri nedir?
İzotop atom özellikleri şu şekilde sıralanabilir. Atom çekirdeğindeki proton sayısı, atom numarası olarak adlandırılır ve nötr atomda bulunan elektron sayısına eşittir. Her bir atom numarası izotopu değil özel bir maddeyi temsil eder. Belli bir maddenin atomundaki nötron sayıları değişiklik gösterebilir. Çekirdekteki nükleon sayısı atomun kütle numarasıdır ve maddenin her bir izotopu farklı kütle numarasına sahiptir.
Örneğin Karbon-12, Karbon-13 ve Karbon-14, karbon maddesinin kütle numaraları sırayla 12, 13 ve 14 olan üç izotopudur. Karbon-6 atom numarası, her bir karbon atomunun 6 protonu vardır anlamına gelir. Bu üç izotopun nötron sayıları sırayla 6,7 ve 8’dir.
Karbon ayak izi nedir?
İzotop formülü nedir?
Bir izotop, tire işareti ve kütle numarasına sahip (helyum-3,helyum-4,karbon-12 gibi) belli bir maddenin adı (atom numarası) ile gösterilir. Örneğin bir kimya sembolü (Mesela karbon için ‘C’) kullanıldığında bilimsel gösterimi, kimyasal sembolün sol üst köşedeki alt simgesi kütle numarasını ve sol alt köşedeki alt simge ise atom numarasını belirtir. Atom numarası maddenin sembolü ile gösterildiğinden, alt simgede genellikle kütle numarası gösterilir ve atom numarası alt simgesi hariç tutulur. Bazı durumlarda kütle numarasının sonuna iliştirilen ‘m’ sembolü, nükleer izomer ya da yarı kararlılığı simgeler.
İzotop çeşitleri nelerdir?
İzotop çeşitleri radyoaktif, ilkel ve durağandır. Bazı izotoplar radyoaktiftir ve bunlara radyonüklit ya da radyoizotop adı verilir. Radyoaktif özellikleri bulunmayan izotoplar durağan izotop yad a durağan nüklit olarak adlandırılır.
İlkel izotoplar yarılanma süresi uzun (100 milyonun üzerinde) 32 nüklit içerir. İlkel izotopların 253 türü durağan izotop olarak sınıflandırılır.
Siyanür nedir?
Doğada izotop mevcudiyeti
Maddeler bir nüklit ya da daha doğal oluşan izotoplardan meydana gelir. Durağan olmayan radyoaktif izotoplar ilkel ve ilkel olmayan şeklinde bulunabilir.
İlkel izotoplar, yıldız nükleosentez ya da kozmik ışın parçalanması gibi başak bir nükleosentez türünün ürünüdür ve sönüm hızı son derece yavaş olduğu için günümüze kadar devamlılık göstermiştir. (Uranyum-238 ve potasyum-40 gibi).
İlkel olmayan izotoplar, kozmojenik nüklit gibi kosmik ışın bombardımanı (karbon-14 gibi) ya da radyoaktif ilkel izotopun zayıflayarak bir radyoaktif radyojenik nüklite (uranyumdan radyuma) sayesinde oluşmuştur.
Birkaç izotop, diğer doğal nükleer reaksiyonlarla doğal olarak nükleojenik nüklit biçiminde sentezlenmiştir. Bu gibi durumlar doğal nükleer fisyondaki nötronların bir başka atom tarafından yutulunca gerçekleşir.
Yalnızca 80 maddenin durağan izotopları bulunmaktadır ve bu 80 maddenin 26’sı tek durağan izotopa sahiptir.Bu sebeple durağan maddelerin yalnızca üçte ikisi Dünya’da doğal olarak oluşabilir. Dünya’da doğal olarak bulunan 94 madde vardır. Bu maddelerden bazıları çok az miktarda mevcuttur. Bilim insanlarına göre Dünya üzerinde oluşabilen izotop sayısının toplamı 339’dur.